Bonjour à toutes et tous.
Comme promis, il est l'heure de revenir sur les deux questions que je vous ai posé hier et sur les réponses apportées.
#thread
(1/24) https://twitter.com/astropierre/status/1303700462248624128
Comme promis, il est l'heure de revenir sur les deux questions que je vous ai posé hier et sur les réponses apportées.
#thread
(1/24) https://twitter.com/astropierre/status/1303700462248624128
Petit disclaimer.
Ce thread n'est pas destiné à rentrer à fond dans tous les détails de la chimie et de la physique.
Mes réponses sont destinées à du grand public et ont pour objectif d'être les plus simples et claires possible, quitte à faire quelques approximations assumées.
Ce thread n'est pas destiné à rentrer à fond dans tous les détails de la chimie et de la physique.
Mes réponses sont destinées à du grand public et ont pour objectif d'être les plus simples et claires possible, quitte à faire quelques approximations assumées.
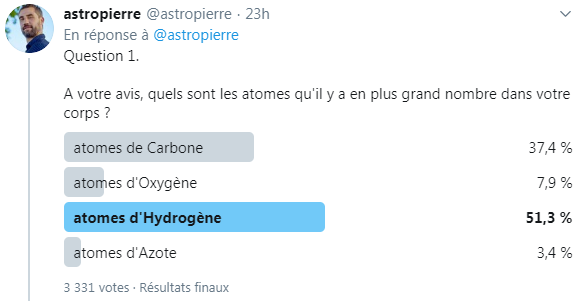
A la première question : "A votre avis, quels sont les atomes qu'il y a en plus grand nombre dans votre corps ?", vous oscillez visiblement entre les atomes de carbone et les atomes d'hydrogène.
Lorsqu'on parle de la vie (au moins celle qui existe sur Terre), on parle effectivement souvent du carbone. En effet, cet atome est, disons, à la base de l'édifice chimique du vivant.
La chimie des molécules contenant du carbone est d'ailleurs appelée "chimie organique".
MAIS
La chimie des molécules contenant du carbone est d'ailleurs appelée "chimie organique".
MAIS
Si l'on compte le nombre d'atomes présents dans le corps, l'hydrogène arrive 1er de très loin.
Votre corps est effectivement composé de:
- 62% d'atomes d'hydrogène
- 24% d'oxygène
- 12% de carbone
- 1,1% d'azote
les 0,9% restants sont emplis de tout le reste (Ca, P, S, K, Na..)
Votre corps est effectivement composé de:
- 62% d'atomes d'hydrogène
- 24% d'oxygène
- 12% de carbone
- 1,1% d'azote
les 0,9% restants sont emplis de tout le reste (Ca, P, S, K, Na..)
...et ce n'est pas très surprenant.
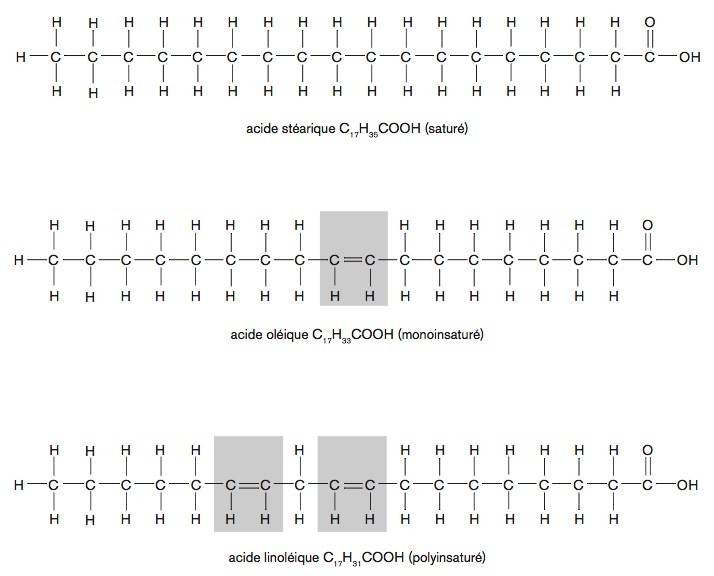
Outre le fait que votre corps est majoritairement composé d'eau (un atome d'oxygène et 2 atomes d'hydrogène), beaucoup de molécules organiques (à base de carbone, donc) sont, elles aussi, bourrées d'hydrogène.
Outre le fait que votre corps est majoritairement composé d'eau (un atome d'oxygène et 2 atomes d'hydrogène), beaucoup de molécules organiques (à base de carbone, donc) sont, elles aussi, bourrées d'hydrogène.
Vous êtes donc, en nombre d'atomes, principalement composés d'hydrogène.
Petite remarque : l'élément hydrogène a été créé, il y a 13.8 milliards d'années, juste après le Big Bang.
Votre corps ayant l'age de ses atomes, vous êtes donc "agés" de 13.8 milliards d'années.



Petite remarque : l'élément hydrogène a été créé, il y a 13.8 milliards d'années, juste après le Big Bang.
Votre corps ayant l'age de ses atomes, vous êtes donc "agés" de 13.8 milliards d'années.




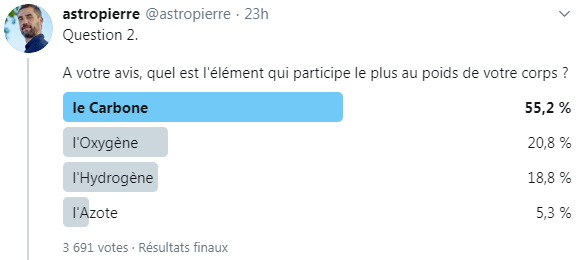
Passons maintenant à la deuxième question : "A votre avis, quel est l'élément qui participe le plus au poids de votre corps ?"
Là encore les réponses sont très intéressantes.
Là encore les réponses sont très intéressantes.
Petite remarque, j'aurais pu (dû ?) utiliser le terme de masse au lieu de poids.
En effet, le poids dépend de l'astre sur lequel on se trouve, la masse (la quantité de matière qui nous compose) non.
Mais dans le problème qui nous occupe, ça ne fait pas beaucoup de différence.
En effet, le poids dépend de l'astre sur lequel on se trouve, la masse (la quantité de matière qui nous compose) non.
Mais dans le problème qui nous occupe, ça ne fait pas beaucoup de différence.
Sur cette 2ème question, le consensus semble être assez clair.
D'après vous, c'est le carbone contenu dans votre corps qui lui donne l'essentiel de sa masse, suivi ensuite par l'oxygène... ou l'hydrogène (quand à l'azote, le pauvre, il est boudé par tout le monde ^^).
D'après vous, c'est le carbone contenu dans votre corps qui lui donne l'essentiel de sa masse, suivi ensuite par l'oxygène... ou l'hydrogène (quand à l'azote, le pauvre, il est boudé par tout le monde ^^).
Intuitivement, ici, on comprend bien que le nombre d'atomes dans le corps n'est plus le seul paramètre à prendre en compte.
La masse de ces atomes est tout aussi importante.
En effet, qu'arrive-t-il si vous avez moins d'atomes, mais qu'ils sont plus massifs que les autres ?...
La masse de ces atomes est tout aussi importante.
En effet, qu'arrive-t-il si vous avez moins d'atomes, mais qu'ils sont plus massifs que les autres ?...
Parlons donc de la masse des ces 4 atomes.
Vous le savez, un atome est composé d'un noyau et de tout petits électrons tout autour.
Ces électrons ont une masse tellement faible qu'en première approximation, on peut dire que la masse d'un atome est égale à celle de son noyau.
Vous le savez, un atome est composé d'un noyau et de tout petits électrons tout autour.
Ces électrons ont une masse tellement faible qu'en première approximation, on peut dire que la masse d'un atome est égale à celle de son noyau.
Ces noyaux, eux, sont composés de particules plus petites encore qu'on appelle "nucléons".
Pas besoin d'aller plus bas pour notre question, on va en rester là.
Alors : De combien de nucléons sont composés les noyaux des atomes de carbone, oxygène, hydrogène et azote ?
Pas besoin d'aller plus bas pour notre question, on va en rester là.
Alors : De combien de nucléons sont composés les noyaux des atomes de carbone, oxygène, hydrogène et azote ?
Hydrogène : 1 nucléon
Carbone : 12 nucléons
Azote : 14 nucléons
Oxygène : 16 nucléons
Eh oui, l'atome d'oxygène est plus massif que l'atome de carbone !
(et non, je ne parlerai pas des isotopes ici )
)
Carbone : 12 nucléons
Azote : 14 nucléons
Oxygène : 16 nucléons
Eh oui, l'atome d'oxygène est plus massif que l'atome de carbone !
(et non, je ne parlerai pas des isotopes ici
 )
)
La 1ère réponse nous avait montré qu'il y a beaucoup plus d'atomes d'Hydrogène dans le corps humain (62%) que d'atomes d'oxygène (24%)
Mais comme les atomes d'oxygène sont ~12 fois plus lourds que l'hydrogène, est-ce qu'ils contribuent plus à sa masse que l'hydrogène ?
Mais comme les atomes d'oxygène sont ~12 fois plus lourds que l'hydrogène, est-ce qu'ils contribuent plus à sa masse que l'hydrogène ?
Eh bien la réponse est OUI !
En terme de masse, les 4 éléments chimiques sont répartis comme tel dans le corps humain :
Oxygène : 61% de la masse du corps humain
Carbone : 23%
Hydrogène : 10%
Azote : 2,6 %
C'est donc bien l'oxygène qui contribue le + à la masse de votre corps.
En terme de masse, les 4 éléments chimiques sont répartis comme tel dans le corps humain :
Oxygène : 61% de la masse du corps humain
Carbone : 23%
Hydrogène : 10%
Azote : 2,6 %
C'est donc bien l'oxygène qui contribue le + à la masse de votre corps.
En d'autre termes, et pour revenir à des quantités plus parlantes, un humain adulte de 70 kg est fait de :
43 kg d'oxygène
16 kg de carbone
7 kg d'hydrogène
1,8 kg d'Azote
allez, je continue
1 kg de calcium
780 g de phosphore
140 g de soufre
140 g de potassium
100 g de sodium
43 kg d'oxygène
16 kg de carbone
7 kg d'hydrogène
1,8 kg d'Azote
allez, je continue
1 kg de calcium
780 g de phosphore
140 g de soufre
140 g de potassium
100 g de sodium
Toutes ces informations (et bien plus encore) peuvent être trouvées dans le "CRC Handbook of Chemistry and Physics", réédité chaque année, dans lequel se trouvent toutes les constantes et grandeurs utilisées en physique, chimie, thermodynamique, mécanique des fluides etc.
Juste avant de clore ce fil, vous vous demandez peut-être :
"A quoi ça sert de connaître la composition chimique d'un être humain ? On n'est pas dans Fullmetal Alchemist, ici !".
"A quoi ça sert de connaître la composition chimique d'un être humain ? On n'est pas dans Fullmetal Alchemist, ici !".
C'est juste.
Toutefois, la connaissance de cette composition, plus qu'importante, peut littéralement vous sauver la vie.
Par exemple, dans un domaine malheureusement encore très actif : le traitement du (des) cancer(s).
Toutefois, la connaissance de cette composition, plus qu'importante, peut littéralement vous sauver la vie.
Par exemple, dans un domaine malheureusement encore très actif : le traitement du (des) cancer(s).
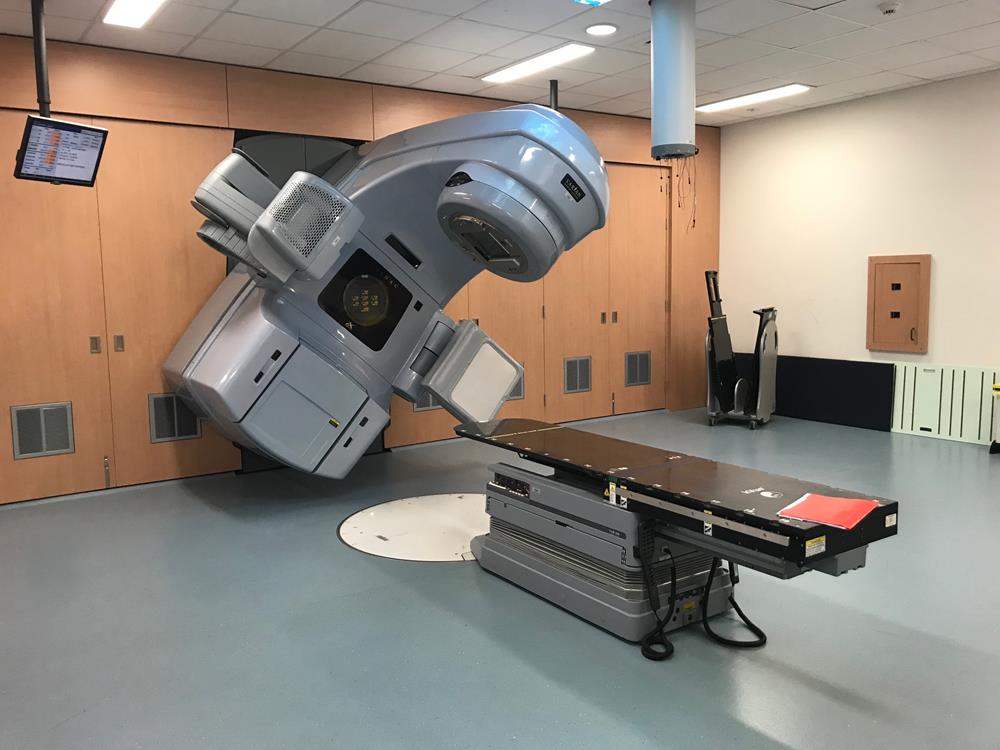
En effet, l'un des traitements de routine contre certains types de cancers est la radiothérapie.
Cela consiste en une irradiation des tissus cancéreux par un ou des faisceau(x) de rayons X, destinés à tuer les cellules cancéreuse et réduire ou faire disparaître la tumeur.
Cela consiste en une irradiation des tissus cancéreux par un ou des faisceau(x) de rayons X, destinés à tuer les cellules cancéreuse et réduire ou faire disparaître la tumeur.
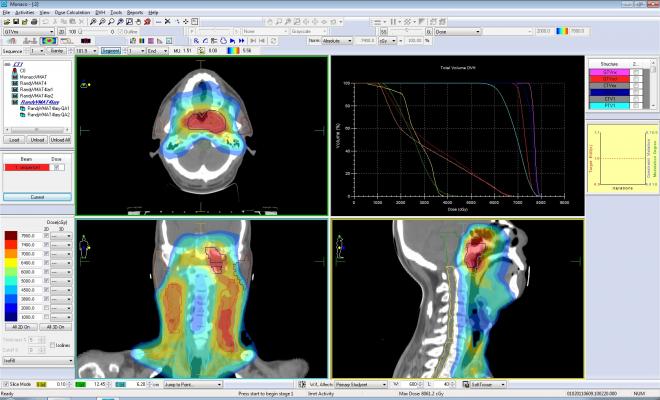
Et pour savoir précisément où irradier, sous quel angle et pendant combien de temps, on dispose de logiciels de planification de traitement qui permettent de simuler ces séances et de trouver les paramètres optimums.
Et bien évidemment, les rayonnements utilisés réagissent différemment en fonction de la composition chimique des différents tissus traversés, d'où la nécessité de connaître avec le plus de précision possible la composition de tous ces tissus.
Sur ce, merci d'avoir lu ce fil jusqu'au bout et bonne fin de journée à toutes et tous.



 Read on Twitter
Read on Twitter